Antonio LUCENA-CACACE
特任准教授(常勤)
大阪大学ヒューマン・メタバース疾患研究拠点
PRIMeの研究者
PRIMeでは、多様な分野、国籍、背景を持つ研究者がアンダーワンルーフで混ざり合い、学際的・統合的な研究ができる研究環境を醸成していきます。

Antonio LUCENA-CACACE
特任准教授(常勤)
大阪大学ヒューマン・メタバース疾患研究拠点
細胞の可塑性と疾患における細胞周期ダイナミクス
私は発生と疾患の基本的な生物学的メカニズムを理解することに深い関心があり、特にヒト人工多能性幹細胞(iPS細胞)の臨床応用に情熱を注いでいます。このモチベーションは、私の研究、特に細胞系譜コミットメント(cell lineage commitment)・拘束・再生・恒常性・老化に影響を与える方法としての細胞周期の制御に焦点を当てた研究の基盤になっています。基礎研究と応用研究の双方で、iPS細胞を最大限に活用するための新しいアイデアを常に探しています。
PRIMeでは、健康状態や疾患状態における生物学的プロセスを再現するために、iPS細胞由来のオルガノイドモデルを用いることに特に関心を寄せています。オルガノイドの再生可能性と予測能力に魅力を感じており、様々な刺激に対するダイナミックな反応を調査しデジタル化してバイオデジタルツインを作成することも研究しています。私の研究の目標は、細胞の恒常性の乱れがどのようにして致命的な結果をもたらす疾患につながるのか、あるいは再生医学の道を開くのかを解明することです。
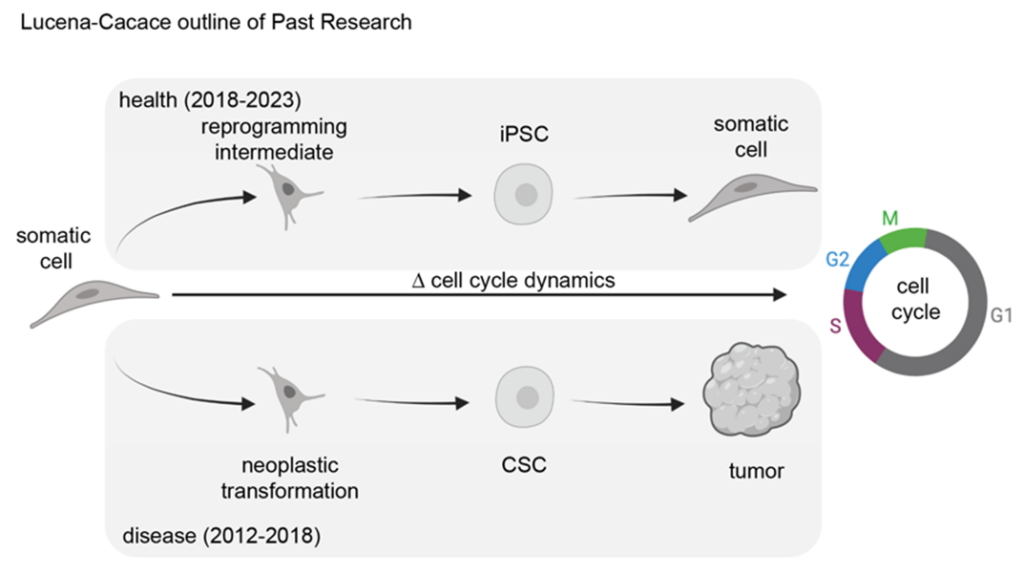
これまでの成果
科学者としてのキャリアが浅いうちは、主に細胞周期ダイナミクスと腫瘍形成におけるその役割の研究に重点を置いていました。具体的には、大腸腫瘍と脳腫瘍におけるNAMPTの機能についてです。私の研究は腫瘍生物学に集中し、NAMPTが腫瘍のリプログラミングと多能性にどのように寄与し、腫瘍の再発を再構成できるがん幹細胞の維持につながっているのかを解明することを目的としていました。私は、がんにおける腫瘍の可塑性と初期化の生物学が、iPS細胞につながる体細胞の初期化と共通することを発見しました。ポスドクとして、また若い教員として私は細胞周期ダイナミクスの研究を続けることを決心し、ヒトiPS細胞が再生するためにどのように体細胞由来に分化できるかに焦点を当てました。2018年以降(図1)、私は研究を以下の5つのセクションに分けています: